بافتهایی که ترمیم میشوند
مقدمه
در سالهای اخیر، توجه به فرآیندهای بازسازی و ترمیم بافتها در بدن به عنوان یکی از مهمترین حوزههای علوم پزشکی و مهندسی بافت افزایش چشمگیری یافته است. بدن انسان به طور طبیعی توانایی ترمیم برخی از بافتهای خود را دارد، اما این قابلیت در بافتهای مختلف متفاوت است. در برخی از بافتها مانند پوست و کبد، فرآیند بازسازی به صورت فعال و گسترده انجام میشود و در بافتهایی دیگر، این توانایی بسیار محدود یا غیرقابل توجه است.
بازسازی بافت به معنای بازتولید ساختار و عملکرد اصلی بافت آسیبدیده است، به طوری که نه تنها نقصها ترمیم شوند، بلکه کارایی طبیعی بافت نیز به طور کامل بازیابی شود. در مقابل، ترمیم بافت بیشتر به فرآیندهای ترمیم زخمی و جایگزینی بافت آسیبدیده با بافتی جدید، که ممکن است ویژگیهای عملکردی مشابه بافت اصلی را نداشته باشد، اشاره دارد. تمایز این دو مفهوم از اهمیت بالایی برخوردار است، زیرا در بازسازی، هدف رسیدن به بازگشت کامل عملکرد است، در حالی که ترمیم ممکن است منجر به ایجاد اسکار یا بافت جایگزین شود که کیفیت عملکردی کمتری دارد.
از سوی دیگر، سلولهای بنیادی نقش بسیار کلیدی و محوری در فرآیندهای بازسازی ایفا میکنند. این سلولها با توانایی تکثیر و تمایز به انواع سلولهای تخصصی، میتوانند به عنوان یک منبع بالقوه برای بازسازی بافتهای آسیبدیده در نظر گرفته شوند. مطالعات گسترده در حوزه سلولهای بنیادی و مهندسی بافت نشان داده است که ترکیب این سلولها با فناوریهای نوین، میتواند افقهای تازهای در درمان بیماریهای صعبالعلاج و آسیبهای شدید ایجاد کند.
در این مقاله، سعی شده است تا یک مرور جامع و تخصصی درباره بافتهای بازسازیشونده در بدن، مکانیزمهای ترمیمی آنها، و بهویژه نقش بیبدیل سلولهای بنیادی در فرآیندهای بازسازی ارائه شود. همچنین، به بررسی فناوریها و روشهای نوین در مهندسی بافت و پزشکی بازساختی پرداخته خواهد شد تا تصویری کامل از وضعیت کنونی و چشمانداز آینده این حوزه فراهم آید.
بافتهای بازسازیشونده در بدن
بدن انسان از بافتهای متنوعی تشکیل شده است که هر کدام ویژگیها و تواناییهای خاصی در زمینه بازسازی و ترمیم دارند. شناخت این تفاوتها برای درک فرآیندهای طبیعی بازسازی و توسعه درمانهای موثر بسیار حیاتی است. در این بخش، به بررسی بافتهایی پرداخته میشود که قابلیت بازسازی چشمگیر و اثربخشی بالایی دارند.
پوست، یکی از بارزترین بافتهای بازسازیشونده
پوست به عنوان بزرگترین اندام بدن، به طور مداوم در معرض آسیبهای محیطی، عفونتها و زخمها قرار دارد. خوشبختانه پوست دارای توانایی بالایی در بازسازی است که این ویژگی به دلیل وجود سلولهای بنیادی در لایههای عمقی و ساختارهای تخصصی مانند فولیکولهای مو و غدد چربی میباشد. هنگام آسیبدیدگی، فرآیند بازسازی پوست شامل فعال شدن سلولهای بنیادی، مهاجرت و تکثیر سلولی و تشکیل بافت جدید است. این فرآیند به گونهای تنظیم میشود که علاوه بر ترمیم سطحی، عملکرد حفاظتی پوست نیز حفظ شود. تحقیقات جدید در زمینه مهندسی بافت پوستی، روشهایی مانند کشت سلولهای بنیادی پوستی و استفاده از داربستهای زیستی را برای بهبود و تسریع این بازسازی معرفی کردهاند.
کبد، نمونهای شاخص از بازسازی درونی و پیچیده
کبد یکی از معدود ارگانهایی است که توانایی بازسازی بافتی فوقالعادهای دارد. حتی پس از برداشت بخش بزرگی از کبد، این اندام قادر است حجم و عملکرد خود را در مدت زمان کوتاهی بازگرداند. این ویژگی به دلیل وجود سلولهای کبدی بالغ و همچنین سلولهای بنیادی اختصاصی کبدی است که در صورت نیاز، به سرعت فعال شده و تمایز مییابند. بازسازی کبد شامل بازسازی ساختارهای پیچیدهای مانند سلولهای پارانشیمایی و عروقی است. این روند نه تنها بازسازی سلولی بلکه تنظیم دقیق پاسخهای التهابی و ترمیمی را نیز در بر میگیرد. مطالعات جدید به بررسی نقش سیگنالهای مولکولی و مسیرهای تنظیمی مانند مسیر Wnt در تنظیم این فرآیندها پرداختهاند.
بافتهای خونی و سیستم ایمنی، بازسازی مستمر و حیاتی
خون و سلولهای سیستم ایمنی نمونههای دیگری از بافتهای بازسازیشونده در بدن هستند که به طور مداوم تجدید میشوند. سلولهای بنیادی خونساز در مغز استخوان مسئول تولید مستمر انواع سلولهای خونی مانند گلبولهای قرمز، گلبولهای سفید و پلاکتها هستند. این بازسازی پیوسته و منظم برای حفظ عملکرد طبیعی بدن و مقابله با آسیبها و بیماریها ضروری است. عملکرد صحیح این سیستم مستلزم تعادل دقیق بین تولید و مرگ سلولی است که به وسیله سیگنالهای محیطی و مولکولی تنظیم میشود.
بافتهای عضلانی، عصبی و استخوانی: محدودیتها و پتانسیلهای بازسازی
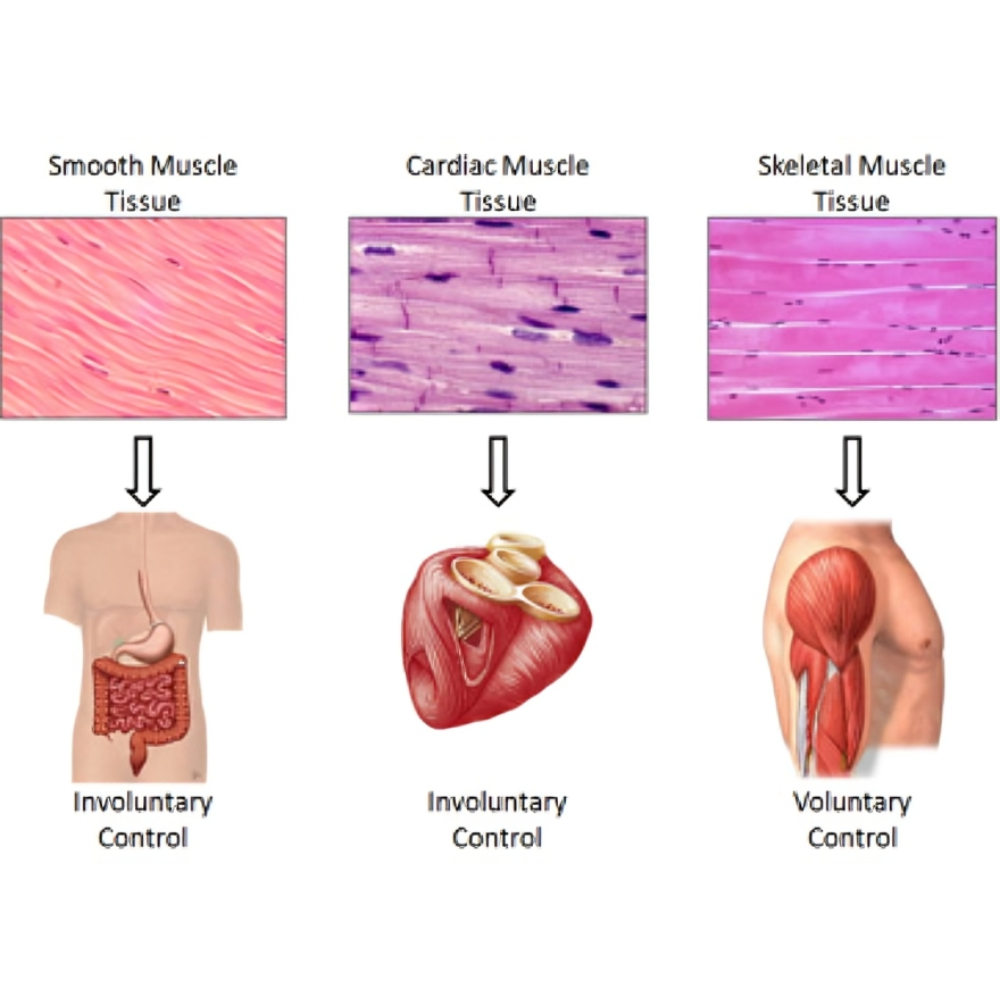
برخی از بافتها مانند عضله اسکلتی، اعصاب محیطی و استخوان نیز دارای توانایی بازسازی هستند، اما این قابلیتها محدودتر و با چالشهای بیشتری همراه است. عضله اسکلتی میتواند با فعال شدن سلولهای ماهیچهای ماهوارهای تا حدی بازسازی شود، اما ترمیم کامل آن در شرایط آسیب شدید یا مزمن ممکن است ناکافی باشد. بافت عصبی مرکزی به دلیل ویژگیهای خاص خود، مانند وجود سد خونی-مغزی و محدودیت در تقسیم سلولی، توانایی بازسازی بسیار محدودی دارد، در حالی که اعصاب محیطی میتوانند تا حدودی پس از آسیب ترمیم شوند. استخوان یکی از بافتهای توانمند در بازسازی است که میتواند شکستگیها و آسیبها را به کمک سلولهای استئوبلاست و فرآیندهای پیچیده بازسازی ساختاری درمان کند.
سلولهای بنیادی و نقش آنها در بازسازی بافت
سلولهای بنیادی، بهعنوان بازیگران کلیدی در بازسازی و ترمیم بافتها، طی چند دهه گذشته به یکی از محورهای اصلی تحقیقات پزشکی تبدیل شدهاند. این سلولها با توانایی منحصر به فرد در تکثیر و تمایز به انواع مختلف سلولهای تخصصی، فرصتهای بینظیری را برای درمان بیماریها و آسیبهای بافتی فراهم کردهاند.
ویژگیهای منحصر به فرد سلولهای بنیادی
سلولهای بنیادی دارای دو ویژگی اصلی هستند که آنها را از دیگر سلولها متمایز میکند: نخست، قابلیت تکثیر نامحدود یا خودنوزایی، و دوم، توانایی تمایز به انواع مختلف سلولهای تخصصی. بسته به منشاء و توان تمایزی، سلولهای بنیادی به چند دسته تقسیم میشوند: سلولهای بنیادی جنینی، سلولهای بنیادی بالغ (مانند سلولهای بنیادی مزانشیمی و خونساز) و سلولهای بنیادی القا شده (iPSCs) که از طریق مهندسی ژنتیکی از سلولهای بالغ تولید میشوند.
نقش سلولهای بنیادی در بازسازی طبیعی بافتها
در شرایط طبیعی، سلولهای بنیادی در حفظ و بازسازی مداوم بافتهایی مانند پوست، خون، و مخاط روده نقش حیاتی دارند. این سلولها در پاسخ به آسیب یا استهلاک سلولی، فعال شده و با تمایز به سلولهای تخصصی، جایگزین سلولهای آسیبدیده میشوند. بهعنوان مثال، در پوست، سلولهای بنیادی در فولیکولهای مو و لایه بازال اپیدرم به طور مستمر نوسازی انجام میدهند. در مغز استخوان، سلولهای بنیادی خونساز، تعادل بین تولید انواع سلولهای خونی را حفظ میکنند.
کاربردهای سلولهای بنیادی در پزشکی بازساختی و درمانهای نوین
سلولهای بنیادی به دلیل توانایی فوقالعادهشان در ترمیم بافتها، به عنوان ابزارهای درمانی در پزشکی بازساختی مورد توجه قرار گرفتهاند. استفاده از سلولهای بنیادی مزانشیمی که از بافتهای مختلفی مانند مغز استخوان، چربی یا پالپ دندان استخراج میشوند، در ترمیم بافتهای آسیبدیده، کاهش التهاب و بهبود عملکرد ارگانها کاربردهای گستردهای یافته است.
در مواردی مانند آسیبهای شدید پوستی، بیماریهای کبدی مزمن و برخی آسیبهای عصبی، پیوند سلولهای بنیادی یا تزریق عوامل ترمیمی مشتق از آنها، باعث تسریع بازسازی و کاهش جای زخم میشود. همچنین، فناوری سلولهای بنیادی القا شده (iPSCs) فرصتهای تازهای برای تولید سلولهای تخصصی بدون محدودیتهای اخلاقی مرتبط با سلولهای جنینی فراهم کرده است.
مکانیسمهای مولکولی فعالشده توسط سلولهای بنیادی در فرآیند بازسازی
سلولهای بنیادی با ترشح فاکتورهای رشد، سایتوکاینها و اجزای خارج سلولی به تنظیم محیط اطراف خود کمک میکنند. این مواد، باعث جذب سلولهای ایمنی، تحریک تکثیر سلولی، و بهبود تشکیل رگهای خونی جدید میشوند. علاوه بر این، مسیرهای سیگنالدهی مهمی مانند مسیر Wnt، Notch و Hedgehog در هدایت تمایز و فعالیت سلولهای بنیادی نقش کلیدی ایفا میکنند.
چالشها و آینده تحقیقات سلولهای بنیادی در بازسازی بافت
با وجود پیشرفتهای چشمگیر، استفاده از سلولهای بنیادی در درمانهای بالینی با چالشهایی همراه است؛ از جمله کنترل دقیق تمایز، جلوگیری از تشکیل تومورهای ناشی از تقسیم سلولی نامنظم، و پاسخ ایمنی بدن به سلولهای پیوندی. در آینده، تحقیقات بر روی توسعه داربستهای زیستی، سیستمهای تحویل هدفمند و ترکیب سلولهای بنیادی با فناوریهای مهندسی بافت، به بهبود اثربخشی درمانها کمک خواهد کرد.
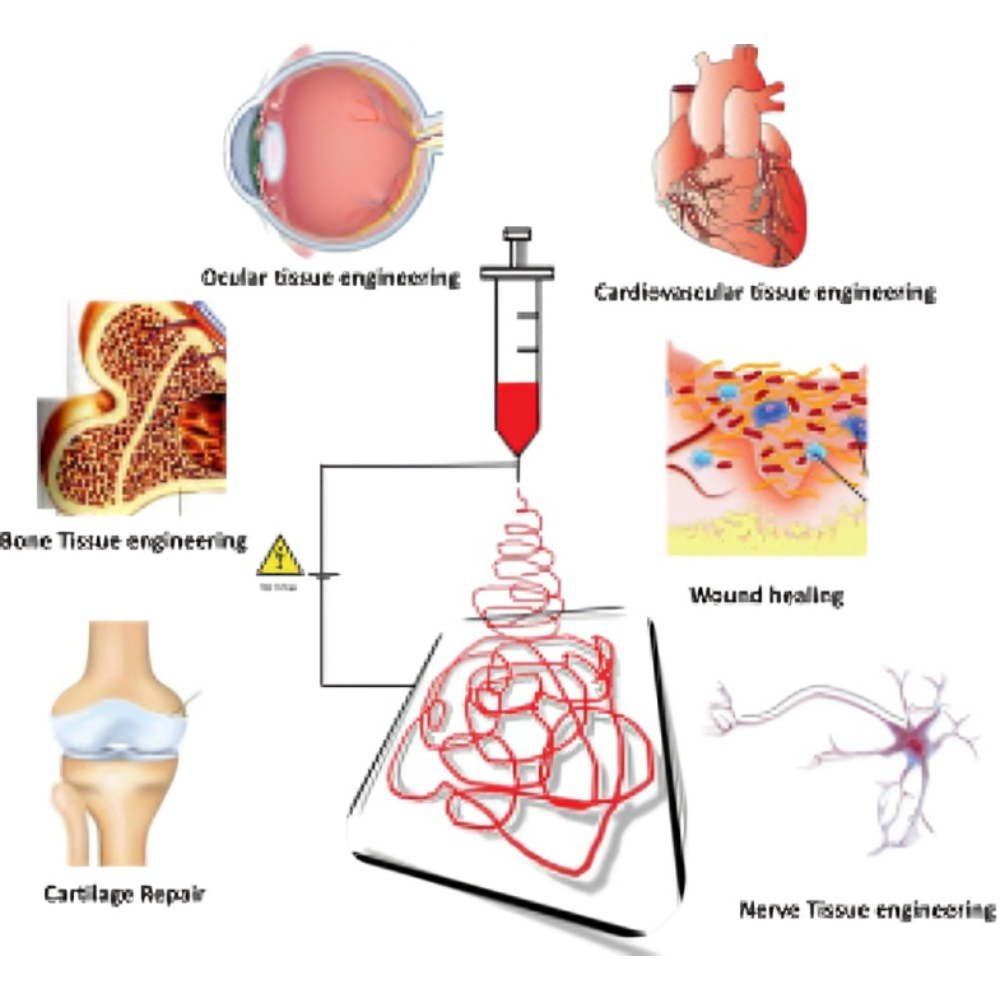
فناوریها و رویکردهای نوین در مهندسی بافت و بازسازی
مهندسی بافت و بازسازی، حوزهای میانرشتهای است که به ترکیب علوم زیستی، مهندسی و پزشکی برای ساخت یا ترمیم بافتها و اندامهای آسیبدیده میپردازد. در سالهای اخیر، پیشرفتهای فناوری و درک عمیقتر از فرآیندهای سلولی و مولکولی، تحول بزرگی در این حوزه ایجاد کرده است که نویدبخش روشهای درمانی پیشرفته و مؤثرتر است.
داربستهای زیستی هوشمند: بستر بازسازی سلولی
یکی از ارکان کلیدی مهندسی بافت، استفاده از داربستهای زیستی است. این داربستها که از مواد طبیعی یا مصنوعی ساخته میشوند، محیطی مناسب برای رشد و تمایز سلولها فراهم میکنند. داربستهای هوشمند قادرند پاسخهای زیستی را تنظیم کنند و حتی در صورت لزوم، عوامل دارویی یا رشد را بهصورت کنترلشده آزاد کنند. برای مثال، استفاده از هیدروژلهای هوشمند که با تغییرات محیطی مثل دما یا pH واکنش نشان میدهند، امکان تنظیم دقیق شرایط رشد سلولها را فراهم میکند.
فناوری چاپ سهبعدی زیستی: ساخت ساختارهای پیچیده بافتی
یکی از دستاوردهای مهم در مهندسی بافت، چاپ سهبعدی زیستی است که به ساخت دقیق و سفارشیسازی بافتها و اندامهای کوچک کمک میکند. در این روش، سلولها به همراه داربستهای زیستی لایه به لایه در قالب سهبعدی قرار میگیرند و ساختاری مشابه بافت طبیعی ایجاد میشود. این فناوری امکان تولید ساختارهای پیچیده مانند پوست چند لایه، بافت استخوان و حتی ساختارهای عروقی را فراهم میآورد.
سلولهای بنیادی در ترکیب با فناوریهای نوین
ترکیب سلولهای بنیادی با داربستهای زیستی و فناوریهای نوین، مانند انتقال ژن و فناوریهای نانو، باعث افزایش تواناییهای بازسازی شده است. برای مثال، داربستهای نانومتری که سطحی مشابه ماتریکس خارجسلولی طبیعی دارند، باعث افزایش چسبندگی و تمایز سلولهای بنیادی میشوند. علاوه بر این، انتقال هدفمند عوامل ژنتیکی میتواند فرآیند تمایز و بازسازی را تسریع کند.
سیستمهای تحویل هدفمند و نانوذرات در بازسازی بافت
استفاده از نانوذرات و سیستمهای تحویل دارو، امکان ارسال دقیق عوامل رشد، ضدالتهاب و سیگنالهای مولکولی به محل آسیبدیده را فراهم کرده است. این فناوریها باعث کاهش عوارض جانبی و افزایش اثربخشی درمان میشوند. همچنین، نانوذرات میتوانند بهعنوان حاملهای سلولهای بنیادی یا عوامل بیولوژیکی عمل کرده و در فرآیند بازسازی نقش کلیدی ایفا کنند.
مهندسی ماتریکس خارجسلولی و مواد بیواکتیو
ماتریکس خارجسلولی (ECM) نقش حیاتی در حفظ ساختار و عملکرد بافتها دارد. مهندسی ECM با استفاده از مواد بیواکتیو، باعث ایجاد محیطی مناسب برای هدایت رشد و تمایز سلولی میشود. این مواد، با فعالسازی مسیرهای سیگنالدهی سلولی، میتوانند پاسخهای بازسازی را بهبود بخشند و فرآیند ترمیم را تسریع کنند.
چالشها و چشمانداز آینده در فناوریهای مهندسی بافت
با وجود پیشرفتهای چشمگیر، مهندسی بافت با چالشهایی مانند تأمین منابع سلولی کافی، پیچیدگی ساختارهای سهبعدی، پاسخ ایمنی بدن و هزینههای بالا مواجه است. آینده این حوزه در گرو توسعه فناوریهای ترکیبی، استفاده از مدلهای پیشرفته آزمایشگاهی و بهکارگیری هوش مصنوعی برای طراحی بهتر داربستها و فرایندهای بازسازی است.
بازسازی پوست: درمان سوختگی و زخمها
پوست به عنوان بزرگترین عضو بدن، نقش حیاتی در حفاظت از بدن در برابر عوامل محیطی، تنظیم دما و حفظ آب بدن دارد. آسیبهای پوستی مانند سوختگیها و زخمها میتوانند باعث اختلال در این عملکردها شده و مشکلات جدی برای فرد ایجاد کنند. بازسازی پوست در این شرایط، یکی از مهمترین چالشهای پزشکی و مهندسی بافت به شمار میآید.
مراحل طبیعی بازسازی پوست
فرآیند ترمیم پوست شامل چند مرحله متوالی است:
-
التهاب اولیه : پس از آسیب، سلولهای ایمنی به محل زخم مهاجرت کرده و عوامل ضدعفونیکننده و رشد را آزاد میکنند.
-
بازسازی بافت : سلولهای فیبروبلاست شروع به تولید ماتریکس خارجسلولی و کلاژن میکنند تا ساختار جدید پوست شکل بگیرد.
-
بازسازی اپیدرم: سلولهای کراتینوسیت از لبههای زخم به سمت مرکز حرکت کرده و لایه اپیدرم را بازسازی میکنند.
-
بازسازی عروقی : رگهای خونی جدید تشکیل میشوند تا خونرسانی مناسب فراهم شود.
با این حال، در زخمهای عمیق یا سوختگیهای شدید، این فرآیند طبیعی کافی نیست و نیاز به مداخلات درمانی تخصصی وجود دارد.
روشهای رایج درمان زخم و سوختگی
درمانهای کلاسیک شامل پیوند پوست، استفاده از پانسمانهای خاص و داروهای ضد التهاب است. با این حال، این روشها محدودیتهایی دارند؛ مانند درد، خطر رد پیوند و اسکارهای ناشی از ترمیم ناکامل.
نقش فناوری مهندسی بافت در بازسازی پوست
امروزه، استفاده از داربستهای زیستی و سلولهای بنیادی در بازسازی پوست، انقلابی در درمان سوختگی و زخمها ایجاد کرده است. این داربستها با فراهم آوردن محیط مناسب برای رشد سلولها و کنترل آزادسازی عوامل رشد، باعث بهبود کیفیت ترمیم و کاهش اسکار میشوند.
سلولهای بنیادی مشتق از پوست و بافتهای دیگر
سلولهای بنیادی پوست و همچنین سلولهای بنیادی مزانشیمی مشتق از بافتهای چربی، نقش مهمی در بازسازی پوست دارند. این سلولها با تمایز به سلولهای پوستی و آزادسازی عوامل رشد، سرعت و کیفیت ترمیم را افزایش میدهند. مطالعات نشان دادهاند که استفاده از این سلولها در درمان سوختگیهای درجه دوم و سوم باعث بهبود چشمگیر نتایج درمانی شده است.
استفاده از پانسمانهای زیستی و هیدروژلها
پانسمانهای زیستی ساخته شده از موادی مانند کیتوزان، کلاژن و هیدروژلها، به عنوان بسترهایی برای رشد سلولها و محافظت از زخم عمل میکنند. این پانسمانها علاوه بر حفظ رطوبت محیط زخم، با آزادسازی کنترل شده عوامل ضد التهاب و ضد باکتری، روند ترمیم را تسریع میکنند.
چاپ سهبعدی پوست: افقهای نوین درمان
یکی از پیشرفتهترین فناوریهای درمان سوختگی و زخم، استفاده از چاپ سهبعدی زیستی پوست است. با این روش، میتوان ساختارهای چندلایهای از سلولهای پوست را در ابعاد و شکلهای مختلف ساخت که با پوست طبیعی همخوانی دارند. این فناوری نویدبخش جایگزینی موثر و سریعتر پوست آسیبدیده است.
چالشها و فرصتهای آینده در بازسازی پوست
با وجود پیشرفتهای قابل توجه، بازسازی کامل پوست با عملکرد و ظاهری طبیعی هنوز با چالشهایی مواجه است. از جمله این مشکلات میتوان به تامین سلولهای مناسب، پاسخ ایمنی و هزینههای بالا اشاره کرد. اما با توسعه فناوریهای جدید، از جمله سلول درمانی، داربستهای هوشمند و نانوفناوری، آینده بازسازی پوست بسیار روشن به نظر میرسد.
بازسازی کبد و نقش سلولهای بنیادی کبدی
کبد یکی از حیاتیترین اندامهای بدن است که مسئولیتهای متعددی از جمله سمزدایی خون، تولید پروتئینهای پلاسما، ذخیره گلیکوژن و سنتز صفرا را بر عهده دارد. قابلیت بازسازی کبد از جمله شگفتیهای بیولوژیکی است که به آن امکان میدهد پس از آسیبهای مختلف، ساختار و عملکرد خود را تا حد زیادی بازیابد.
مکانیزمهای طبیعی بازسازی کبد
کبد به کمک سلولهای هپاتوسیت قادر به بازسازی است. پس از آسیب، این سلولها وارد فاز تکثیر شده و بخشهای از دست رفته بافت کبد جایگزین میشوند. این فرآیند در شرایط آسیبهای خفیف و متوسط بسیار موثر است، اما در موارد آسیب شدید یا مزمن، مانند سیروز یا هپاتیت پیشرفته، توان بازسازی طبیعی کاهش مییابد.
نقش سلولهای بنیادی کبدی در ترمیم و بازسازی
در شرایطی که بازسازی طبیعی کبد کافی نباشد، سلولهای بنیادی کبدی (Liver Stem/Progenitor Cells) وارد عمل میشوند. این سلولها که در بخشهای خاصی از کبد مانند کانالهای صفراوی قرار دارند، قادر به تمایز به سلولهای هپاتوسیت و کلانژیوستها هستند و در ترمیم زخمهای عمیق نقش حیاتی دارند.
ویژگیهای منحصر به فرد سلولهای بنیادی کبدی
این سلولها علاوه بر قابلیت تکثیر بالا، توانایی پاسخ سریع به آسیبهای گسترده را دارند و میتوانند به سرعت در محل آسیب تجمع یابند. تحقیقات نشان دادهاند که تحریک این سلولها با استفاده از عوامل رشد و محیطهای کشت مناسب میتواند روند بازسازی کبد را به شکل قابل توجهی بهبود بخشد.
کاربردهای بالینی و درمانی سلولهای بنیادی کبدی
امروزه، بهرهگیری از تزریق سلولهای بنیادی کبدی یا استفاده از سلولهای بنیادی مزانشیمی مشتق از منابع مختلف به عنوان روشهای نوین درمانی برای بیماریهای کبدی در حال گسترش است. این روشها میتوانند به کاهش التهاب، ترمیم بافت و بهبود عملکرد کبد در بیماران دچار نارسایی کبد کمک کنند.
تحدیدات و چالشهای موجود
با وجود پیشرفتها، کاربرد بالینی سلولهای بنیادی کبدی هنوز با چالشهایی مانند کنترل تمایز سلولی، پاسخ ایمنی و انتقال موثر سلولها مواجه است. علاوه بر این، خطر بالقوه تشکیل تومور و ناپایداری ژنتیکی سلولها نیز مورد توجه پژوهشگران قرار دارد.
آینده پژوهشها و فناوریهای بازسازی کبد
پیشرفت در حوزه مهندسی بافت و فناوریهای سلولی، از جمله تولید کبدهای مصنوعی یا ارگانوییدهای کبدی، نویدبخش راهکارهای درمانی موثرتر و شخصیسازی شده برای بیماران کبدی است. این فناوریها با تلفیق سلولهای بنیادی و داربستهای زیستی، امکان ترمیم سریعتر و عملکردی بهتر کبد را فراهم خواهند کرد.
بازسازی استخوان و بافتهای پیوندی
استخوانها و بافتهای پیوندی نقش بسیار مهمی در ساختار بدن و عملکرد مکانیکی آن دارند. بازسازی این بافتها پس از آسیب یا بیماری، یکی از چالشهای مهم در حوزه پزشکی و مهندسی بافت است. خوشبختانه، بدن انسان دارای تواناییهای طبیعی و مکانیزمهایی است که به بازسازی این بافتها کمک میکند، هرچند در موارد آسیب شدید نیازمند کمک فناوریهای نوین هستیم.
ویژگیهای بازسازی طبیعی استخوان
استخوانها از طریق فرآیندی به نام بازسازی استخوان (bone remodeling) قادر به ترمیم خود هستند. این فرآیند متشکل از دو مرحله اصلی است: ابتدا استئوکلاستها، سلولهای مسئول تجزیه استخوان آسیبدیده را فعال میکنند و سپس استئوبلاستها به ساخت استخوان جدید میپردازند. این تعادل دقیق بین تخریب و ساخت، باعث حفظ سلامت و استحکام استخوان میشود.
بازسازی بافتهای پیوندی
بافتهای پیوندی مانند تاندونها، لیگامانها و غضروفها نیز نقش حیاتی در اتصال استخوانها و ایجاد حرکتهای طبیعی دارند. این بافتها از نظر خونرسانی ضعیفتر بوده و بنابراین توان بازسازی کمتری نسبت به استخوان دارند. این موضوع باعث شده است که درمان آسیبهای بافت پیوندی، به ویژه غضروف، یکی از حوزههای فعال تحقیقاتی در مهندسی بافت باشد.
نقش سلولهای بنیادی در بازسازی استخوان و بافتهای پیوندی
سلولهای بنیادی مزانشیمی (MSCs) که از منابعی مانند مغز استخوان و بافت چربی استخراج میشوند، توانایی تمایز به سلولهای استخوانی، غضروفی و دیگر سلولهای بافت پیوندی را دارند. استفاده از این سلولها در بازسازی بافتهای اسکلتی-عضلانی، روند بهبودی را تسریع کرده و کیفیت بافت ترمیم شده را بهبود میبخشد.
فناوریهای داربست و مواد بیوسازگار در مهندسی بافت استخوان
برای حمایت از رشد سلولها و تشکیل بافت جدید، از داربستهای زیستی استفاده میشود که محیط مناسبی برای چسبندگی، تکثیر و تمایز سلولی فراهم میکنند. این داربستها معمولاً از مواد بیوسازگار و قابل تجزیه مانند کلسیم فسفات، هیدروکسی آپاتیت و پلیمرهای طبیعی یا مصنوعی ساخته میشوند. طراحی مناسب این داربستها، از نظر اندازه منافذ، پایداری مکانیکی و قابلیت جذب، برای موفقیت درمان ضروری است.
تلفیق سلولهای بنیادی و داربستها در درمانهای بالینی
امروزه ترکیب سلولهای بنیادی با داربستهای پیشرفته در آزمایشات بالینی برای ترمیم شکستگیهای پیچیده، نقصهای استخوانی ناشی از بیماری یا آسیبهای ورزشی کاربرد گستردهای یافته است. این روشها میتوانند از بروز نیاز به جراحیهای سنگین مانند پیوند استخوان اتولوگ یا آلوگرافت جلوگیری کنند.
چالشها و محدودیتها
با وجود پیشرفتهای چشمگیر، هنوز چالشهایی مانند کنترل دقیق جهتگیری تمایز سلولی، پاسخهای ایمنی، تامین سلولهای با کیفیت بالا و هزینههای درمان وجود دارد. علاوه بر این، بازسازی کامل بافتهای پیچیدهای مانند مفاصل، که ترکیبی از استخوان، غضروف و بافتهای پیوندی هستند، نیازمند تحقیقات گستردهتر و فناوریهای نوینتر است.
آینده بازسازی استخوان و بافتهای پیوندی
پیشرفت در فناوریهایی مانند چاپ سهبعدی زیستی(3D bioprinting)، نانو فناوری و سیستمهای تحویل هدفمند داروها، افق جدیدی را در بازسازی استخوان و بافتهای پیوندی گشودهاند. انتظار میرود در آینده نزدیک، این فناوریها باعث تولید بافتهای پیچیدهتر و قابل پیوند با کیفیت بالاتر شوند و امکان درمانهای شخصیسازی شده برای بیماران فراهم گردد.
موانع و چالشها در بازسازی بافتها و درمانهای مبتنی بر سلولهای بنیادی
بازسازی بافتها و استفاده از سلولهای بنیادی به عنوان یکی از پیشرفتهترین روشهای درمانی، امیدهای بسیاری را در پزشکی نوین ایجاد کرده است. با این حال، مسیر بالینی شدن این فناوریها و کاربرد گسترده آنها با چالشها و موانع متعددی روبرو است که باید به دقت بررسی و رفع شوند.
محدودیتهای مربوط به تامین و کیفیت سلولهای بنیادی
یکی از بزرگترین چالشها، تأمین سلولهای بنیادی با کیفیت، تعداد کافی و قابلیت تمایز مطلوب است. سلولهای بنیادی مزانشیمی و پرتوان، در شرایط کشت و ذخیرهسازی ممکن است تغییراتی در ویژگیهای خود تجربه کنند که روی اثربخشی درمان اثرگذار است. علاوه بر این، منابع سلولی محدود و پیچیدگی استخراج آنها باعث افزایش هزینهها و زمانبر شدن فرایند درمان میشود.
ریسکهای ایمنی و عوارض جانبی
استفاده از سلولهای بنیادی، به ویژه سلولهای پرتوان القایی (iPSCs)، میتواند با خطراتی همچون تشکیل تومورهای ناخواسته همراه باشد. همچنین پاسخهای ایمنی میزبان به سلولهای پیوندی یا مواد داربست ممکن است منجر به التهاب و پس زدن بافت شود. این مسائل نیازمند مطالعات دقیقتر و توسعه روشهای کنترل ایمنی است.
چالشهای مربوط به محیط زیستی و میکرو محیط سلولی
برای بازسازی موفق بافت، میکرو محیط سلولی باید شرایط مناسب برای بقای سلولها، تکثیر و تمایز آنها را فراهم کند. ایجاد این محیط بهینه، شامل تامین مواد مغذی، اکسیژن، سیگنالهای بیوشیمیایی و مکانیکی، از پیچیدگیهای عمده مهندسی بافت است که هنوز به طور کامل حل نشده است.
مشکلات مربوط به داربستها و فناوریهای همراه
انتخاب داربست مناسب که بتواند به خوبی با سلولها تعامل داشته باشد، ساختار سهبعدی مورد نیاز را فراهم کند و به تدریج در بدن تجزیه شود، یکی از چالشهای کلیدی است. بسیاری از داربستها ممکن است مشکلاتی مانند واکنشهای التهابی، دوام کم یا عدم تجزیه مناسب داشته باشند که اثرگذاری درمان را کاهش میدهد.
محدودیتهای فنی و اقتصادی در تولید و کاربرد بالینی
فرآیندهای کشت سلول، ساخت داربست، و آمادهسازی نهایی درمانهای سلولی نیازمند تجهیزات پیشرفته، نیروی انسانی متخصص و هزینههای بالاست. این محدودیتها باعث شدهاند که بسیاری از روشهای مهندسی بافت در مرحله آزمایشگاهی باقی بمانند و تنها تعداد محدودی وارد بازار درمانی شوند.
موانع قانونی و اخلاقی
کاربرد سلولهای بنیادی، به ویژه آنهایی که از منابع انسانی جنینی استخراج میشوند، با چالشهای قانونی و اخلاقی فراوانی روبرو است. همچنین، عدم وجود چارچوبهای استاندارد و قوانین جامع برای تولید و استفاده از محصولات سلولی، مانع توسعه سریع و ایمن این حوزه شده است.
چشمانداز رفع چالشها
پیشرفتهای اخیر در زمینه بیوتکنولوژی، تولید سلولهای بنیادی پرتوان القایی، بهبود داربستهای زیستی و فناوریهای نوین کشت سهبعدی، نویدبخش حل بسیاری از این مشکلات است. همکاری بینالمللی، تدوین استانداردهای سختگیرانه و افزایش سرمایهگذاری در تحقیق و توسعه میتواند راه را برای تسریع ورود درمانهای بازسازی بافت به عرصه بالینی هموار کند.
چشمانداز آینده و نوآوریهای پیش رو در پزشکی بازساختی
پزشکی بازساختی به عنوان یکی از حوزههای پیشرفته و تحولآفرین در علوم پزشکی، چشماندازهای گستردهای برای درمان بیماریها و آسیبهای پیچیده ارائه میدهد. پیشرفتهای روزافزون در زمینههای مختلف علمی و فناوری نویدبخش توسعه روشهای مؤثرتر، دقیقتر و ایمنتر در بازسازی بافتها و اندامها است.
توسعه سلولهای بنیادی پرتوان القایی و مهندسی ژنتیک
یکی از نوآوریهای کلیدی در آینده پزشکی بازساختی، استفاده گستردهتر از سلولهای بنیادی پرتوان القایی (iPSCs) است. این سلولها، که قابلیت تبدیل به انواع سلولهای تخصصی را دارند، امکان ایجاد درمانهای شخصیسازی شده را فراهم میآورند. همچنین، ترکیب این سلولها با فناوری مهندسی ژنتیک، به ویژه ابزارهای ویرایش ژن مانند CRISPR، میتواند باعث اصلاح نقصهای ژنتیکی و افزایش اثربخشی درمانها شود.
پیشرفت در فناوریهای چاپ سهبعدی زیستی
فناوری چاپ سهبعدی زیستی، به عنوان یکی از نوآوریهای مهم، امکان ساخت داربستهای پیچیده با ساختار سهبعدی دقیق و قابلیت تزریق سلولهای مختلف را فراهم کرده است. این فناوری میتواند منجر به تولید اندامهای مصنوعی یا قطعات بافتی برای پیوند شود که به طور کامل با ویژگیهای زیستی بدن سازگار باشند.
کشت سهبعدی پیشرفته و میکرو محیط زیستی بهینهشده
توسعه روشهای کشت سهبعدی پیشرفته و ایجاد میکرو محیطهای زیستی شبیهسازی شده، کمک میکند تا سلولها در شرایطی نزدیک به محیط طبیعی خود رشد کنند و عملکرد بهتری داشته باشند. این پیشرفتها، به افزایش پایداری و عملکرد درمانهای سلولی کمک شایانی خواهد کرد.
نانو فناوری و داربستهای هوشمند
ادغام نانو فناوری در پزشکی بازساختی، به تولید داربستهای هوشمند و سیستمهای تحویل هدفمند دارو و سلول کمک میکند. این داربستها میتوانند به صورت کنترلشده به محیط هدف پاسخ دهند و روند بهبودی را تسریع کنند.
کاربرد هوش مصنوعی و یادگیری ماشین در طراحی درمانها
هوش مصنوعی و یادگیری ماشین نقش کلیدی در بهبود طراحی داربستها، پیشبینی پاسخهای سلولی و بهینهسازی فرایندهای کشت و درمان ایفا میکنند. این فناوریها باعث میشوند روند توسعه درمانها سریعتر، دقیقتر و اقتصادیتر شود.
افزایش همکاریهای بینرشتهای و توسعه چارچوبهای قانونی و اخلاقی
پیشرفت در پزشکی بازساختی نیازمند همکاری گسترده میان متخصصان بیولوژی، مهندسی، پزشکی، و حقوق است. ایجاد چارچوبهای قانونی و اخلاقی شفاف و منسجم، نقش مهمی در تسهیل ورود فناوریهای نوین به بازار درمان خواهد داشت.
چشمانداز آینده پزشکی بازساختی بسیار امیدوارکننده است و نوآوریهای پیش رو میتوانند مرزهای درمان را گسترش دهند. با تکیه بر پیشرفتهای علمی، فناوریهای نوین و همکاریهای چندرشتهای، انتظار میرود که در دهههای آینده، درمانهای بازساختی به بخش جداییناپذیر و موثر از مراقبتهای پزشکی تبدیل شوند.
نتیجهگیری
پزشکی بازساختی به عنوان یک حوزه علمی نوین، فرصتهای بینظیری را برای درمان بیماریها و آسیبهای بافتی فراهم کرده است. از طریق استفاده از سلولهای بنیادی، فناوریهای پیشرفته مهندسی بافت و نوآوریهای متعدد در زمینههای بیومواد و داربستهای زیستی، توانستهایم به بازسازی و ترمیم بافتهای مختلف بدن نزدیکتر شویم.
با این حال، همانطور که در بخشهای قبلی بررسی شد، چالشها و محدودیتهایی همچون واکنشهای ایمنی، کنترل رشد و تمایز سلولی، و موانع فنی موجود، هنوز نیازمند پژوهش و توسعه بیشتری هستند. همچنین، توجه به جوانب اخلاقی و مقرراتی برای تضمین ایمنی و اثر بخشی درمانها، از اهمیت بالایی برخوردار است.
با تکیه بر پیشرفتهای علمی و فناوری، چشمانداز آینده این حوزه بسیار روشن است و امید میرود که با ترکیب تخصصهای مختلف و حمایتهای پژوهشی، بتوان درمانهای بازساختی را به صورت گسترده و قابل اطمینان در مراقبتهای پزشکی به کار گرفت. در نهایت، پزشکی بازساختی میتواند تحولی اساسی در کیفیت زندگی بیماران ایجاد کند و افقهای نوینی را در درمان بیماریهای لاعلاج و آسیبهای شدید باز کند.